Skandiumi, me simbolin e elementit Sc dhe numrin atomik 21, tretet lehtësisht në ujë, mund të bashkëveprojë me ujin e nxehtë dhe errësohet lehtësisht në ajër. Valenca e tij kryesore është +3. Shpesh përzihet me gadolinium, erbium dhe elementë të tjerë, me një rendiment të ulët dhe një përmbajtje prej afërsisht 0.0005% në kore. Skandiumi përdoret shpesh për të bërë qelq special dhe lidhje të lehta me temperaturë të lartë.
Aktualisht, rezervat e provuara të skandiumit në botë janë vetëm 2 milionë ton, 90~95% e të cilave përmbahen në xehe të boksitit, fosforitit dhe hekurit, titaniumi, dhe një pjesë e vogël në xehe të uraniumit, toriumit, tungstenit dhe metaleve të rralla të tokës, të shpërndara kryesisht në Rusi, Kinë, Taxhikistan, Madagaskar, Norvegji dhe vende të tjera. Kina është shumë e pasur me burime skandiumi, me rezerva të mëdha mineralesh të lidhura me skandiumin. Sipas statistikave të paplota, rezervat e skandiumit në Kinë janë rreth 600000 ton, të cilat përmbahen në depozitat e boksitit dhe fosforitit, depozitat e porfirit dhe venave të kuarcit të tungstenit në Kinën Jugore, depozitat e metaleve të rralla të tokës në Kinën Jugore, depozitat e xehes së hekurit të tokës së rrallë Bayan Obo në Mongolinë e Brendshme dhe depozitat e magnetitit të vanadiumit dhe titaniumi Panzhihua në Sichuan.
Për shkak të mungesës së skandiumit, çmimi i skandiumit është gjithashtu shumë i lartë, dhe në kulmin e tij, çmimi i skandiumit u fry në 10 herë çmimin e arit. Edhe pse çmimi i skandiumit ka rënë, ai është ende katër herë më i lartë se çmimi i arit!
Zbulimi i Historisë
Në vitin 1869, Mendeleev vuri re një boshllëk në masën atomike midis kalciumit (40) dhe titanit (48), dhe parashikoi se këtu ekzistonte edhe një element i pazbuluar me masë atomike të ndërmjetme. Ai parashikoi se oksidi i tij është X ₂ O Å. Skandiumi u zbulua në vitin 1879 nga Lars Frederik Nilson i Universitetit të Uppsalës në Suedi. Ai e nxori atë nga miniera e rrallë e arit të zi, një xeheror kompleks që përmban 8 lloje oksidesh metalike. Ai ka nxjerrëOksid erbiumi(III)nga xeherori i rrallë i arit të zi dhe i marrëOksid iterbiumi(III)nga ky oksid, dhe ekziston një oksid tjetër i një elementi më të lehtë, spektri i të cilit tregon se është një metal i panjohur. Ky është metali i parashikuar nga Mendeleev, oksidi i të cilit ështëSc₂O₃Vetë metali i skandiumit u prodhua ngaKlorur skandiumime shkrirje elektrolitike në vitin 1937.
Mendeleev
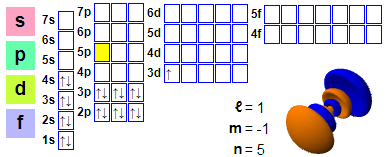
Konfigurimi i elektroneve
Konfigurimi i elektroneve: 1s2 2s2 2p6 3s2 3p6 4s2 3d1
Skandiumi është një metal tranzicioni i butë, i bardhë argjendi me një pikë shkrirjeje prej 1541 ℃ dhe një pikë vlimi prej 2831 ℃.
Për një periudhë të konsiderueshme kohore pas zbulimit të tij, përdorimi i skandiumit nuk u demonstrua për shkak të vështirësisë së tij në prodhim. Me përmirësimin në rritje të metodave të ndarjes së elementeve të rrallë të tokës, tani ekziston një rrjedhë e pjekur e procesit për pastrimin e përbërjeve të skandiumit. Meqenëse skandiumi është më pak alkalik se itriumi dhe lantanidi, hidroksidi është më i dobëti, kështu që minerali i përzier i elementeve të rrallë të tokës që përmban skandium do të ndahet nga elementi i rrallë i tokës me anë të metodës së "precipitimit hap pas hapi" kur hidroksidi i skandiumit (III) trajtohet me amoniak pasi të transferohet në tretësirë. Metoda tjetër është ndarja e nitratit të skandiumit me anë të dekompozimit polar të nitratit. Meqenëse nitrati i skandiumit është më i lehtë për t'u dekompozuar, skandiumi mund të ndahet. Përveç kësaj, rikuperimi gjithëpërfshirës i skandiumit shoqërues nga uraniumi, toriumi, tungsteni, kallaji dhe depozitat e tjera minerale është gjithashtu një burim i rëndësishëm i skandiumit.
Pas marrjes së një përbërjeje të pastër skandiumi, ajo shndërrohet në ScCl Å dhe bashkëshkrihet me KCl dhe LiCl. Zinku i shkrirë përdoret si katodë për elektrolizë, duke bërë që skandiumi të precipitojë në elektrodën e zinkut. Pastaj, zinku avullohet për të marrë skandium metalik. Ky është një metal i lehtë i bardhë argjendi me veti kimike shumë aktive, i cili mund të reagojë me ujë të nxehtë për të gjeneruar gaz hidrogjeni. Pra, skandiumi metalik që shihni në figurë është i mbyllur në një shishe dhe i mbrojtur me gaz argoni, përndryshe skandiumi do të formojë shpejt një shtresë oksidi të verdhë të errët ose gri, duke humbur shkëlqimin e tij metalik të shndritshëm.
Aplikacionet
Industria e ndriçimit
Përdorimet e skandiumit janë të përqendruara në drejtime shumë të ndritshme, dhe nuk është ekzagjerim ta quajmë Biri i Dritës. Arma e parë magjike e skandiumit quhet llambë natriumi skandiumi, e cila mund të përdoret për të sjellë dritë në mijëra familje. Kjo është një dritë elektrike halide metali: llamba është e mbushur me jodur natriumi dhe trijodur skandiumi, dhe skandiumi dhe petë natriumi shtohen në të njëjtën kohë. Gjatë shkarkimit me tension të lartë, jonet e skandiumit dhe jonet e natriumit lëshojnë përkatësisht dritë me gjatësi vale karakteristike të emetimit të tyre. Vijat spektrale të natriumit janë 589.0 dhe 589.6 nm, dy drita të famshme të verdha, ndërsa vijat spektrale të skandiumit janë 361.3~424.7 nm, një seri emetimesh të dritës afër ultravjollcë dhe blu. Meqenëse ato plotësojnë njëra-tjetrën, ngjyra e përgjithshme e dritës së prodhuar është dritë e bardhë. Pikërisht për shkak se llambat me skandium natriumi kanë karakteristikat e efikasitetit të lartë ndriçues, ngjyrës së mirë të dritës, kursimit të energjisë, jetëgjatësisë së gjatë të shërbimit dhe aftësisë së fortë për të thyer mjegullën, ato mund të përdoren gjerësisht për kamerat televizive, sheshet, mjediset sportive dhe ndriçimin rrugor, dhe njihen si burimet e dritës së gjeneratës së tretë. Në Kinë, ky lloj llambë po promovohet gradualisht si një teknologji e re, ndërsa në disa vende të zhvilluara, ky lloj llambë është përdorur gjerësisht që në fillim të viteve 1980.
Arma e dytë magjike e skandiumit janë qelizat fotovoltaike diellore, të cilat mund të mbledhin dritën e shpërndarë në tokë dhe ta shndërrojnë atë në energji elektrike për të vënë në lëvizje shoqërinë njerëzore. Skandiumi është metali më i mirë pengues në qelizat diellore të silikonit gjysmëpërçues, izolator metalik dhe qelizat diellore.
Arma e saj e tretë magjike quhet burim rrezesh γ. Ky armë magjike mund të shkëlqejë shkëlqyeshëm vetë, por ky lloj drite nuk mund të perceptohet me sy të lirë, është një rrjedhë fotoni me energji të lartë. Zakonisht nxjerrim 45Sc nga mineralet, i cili është i vetmi izotop natyror i skandiumit. Çdo bërthamë 45Sc përmban 21 protone dhe 24 neutrone. 46Sc, një izotop radioaktiv artificial, mund të përdoret si burim rrezatimi γ ose atome gjurmuese që mund të përdoren gjithashtu për radioterapinë e tumoreve malinje. Ekzistojnë gjithashtu aplikime si lazeri i itritiumit, galiumit, skandiumit dhe granatit.Fluoridi i skandiumitFibër optike me infra të kuqe qelqi dhe tub katodik i veshur me skandium në televizion. Duket se skandiumi lind me shkëlqim.
Industria e aliazheve
Skandiumi në formën e tij elementare është përdorur gjerësisht për dopingun e lidhjeve të aluminit. Për sa kohë që aluminit i shtohen disa të mijëta të skandiumit, do të formohet një fazë e re Al3Sc, e cila do të luajë një rol metamorfizues në lidhjen e aluminit dhe do të bëjë që struktura dhe vetitë e lidhjes të ndryshojnë ndjeshëm. Shtimi i 0.2%~0.4% Sc (që është shumë i ngjashëm me proporcionin e shtimit të kripës në perimet e skuqura në shtëpi, nevojitet vetëm pak) mund të rrisë temperaturën e rikristalizimit të lidhjes me 150-200 ℃, dhe të përmirësojë ndjeshëm forcën në temperaturë të lartë, stabilitetin strukturor, performancën e saldimit dhe rezistencën ndaj korrozionit. Gjithashtu mund të shmangë fenomenin e brishtësisë që është i lehtë për t'u shfaqur gjatë punës afatgjatë në temperatura të larta. Lidhja e aluminit me rezistencë të lartë dhe rezistencë të lartë, lidhja e re e aluminit e saldueshme me rezistencë të lartë ndaj korrozionit, lidhja e re e aluminit me temperaturë të lartë, lidhja e aluminit rezistente ndaj rrezatimit të neutroneve me rezistencë të lartë, etj., kanë perspektiva shumë tërheqëse zhvillimi në hapësirën ajrore, aviacionin, anijet, reaktorët bërthamorë, automjetet e lehta dhe trenat me shpejtësi të lartë.
Skandiumi është gjithashtu një modifikues i shkëlqyer për hekurin, dhe një sasi e vogël skandiumi mund të përmirësojë ndjeshëm forcën dhe fortësinë e gizës. Përveç kësaj, skandiumi mund të përdoret gjithashtu si një shtesë për lidhjet e tungstenit dhe kromit me temperaturë të lartë. Sigurisht, përveç prodhimit të rrobave të dasmës për të tjerët, skandiumi ka një pikë të lartë shkrirjeje dhe dendësia e tij është e ngjashme me atë të aluminit, dhe përdoret gjithashtu në lidhjet e lehta me pikë të lartë shkrirjeje, siç janë lidhja e titaniumit dhe skandiumit. Megjithatë, për shkak të çmimit të tij të lartë, ai përdoret përgjithësisht vetëm në industri prodhuese të nivelit të lartë, siç janë anijet kozmike dhe raketat.
Material qeramik
Skandiumi, një substancë e vetme, përdoret përgjithësisht në lidhje, dhe oksidet e tij luajnë një rol të rëndësishëm në materialet qeramike në një mënyrë të ngjashme. Materiali qeramik tetragonal i zirkonit, i cili mund të përdoret si material elektrode për qelizat e karburantit me oksid të ngurtë, ka një veti unike ku përçueshmëria e këtij elektroliti rritet me rritjen e temperaturës dhe përqendrimit të oksigjenit në mjedis. Megjithatë, struktura kristalore e këtij materiali qeramik në vetvete nuk mund të ekzistojë në mënyrë të qëndrueshme dhe nuk ka vlerë industriale; Është e nevojshme të shtohen disa substanca që mund ta fiksojnë këtë strukturë në mënyrë që të ruhen vetitë e saj origjinale. Shtimi i 6~10% oksid skandiumi është si një strukturë betoni, në mënyrë që zirkonia të mund të stabilizohet në një rrjetë katrore.
Ekzistojnë gjithashtu materiale qeramike inxhinierike, të tilla si nitridi i silikonit me rezistencë të lartë dhe ndaj temperaturave të larta, si dendësues dhe stabilizues.
Si një dendësues,Oksid skandiumimund të formojë një fazë zjarrduruese Sc2Si2O7 në buzë të grimcave të imëta, duke zvogëluar kështu deformimin e temperaturës së lartë të qeramikës inxhinierike. Krahasuar me oksidet e tjera, mund të përmirësojë më mirë vetitë mekanike të temperaturës së lartë të nitritit të silikonit.
Kimi katalitike
Në inxhinierinë kimike, skandiumi përdoret shpesh si katalizator, ndërsa Sc2O3 mund të përdoret për dehidratimin dhe deoksidimin e etanolit ose izopropanolit, zbërthimin e acidit acetik dhe prodhimin e etilenit nga CO dhe H2. Katalizatori PtAl që përmban Sc2O3 është gjithashtu një katalizator i rëndësishëm për proceset e pastrimit dhe rafinimit të hidrogjenizimit të naftës së rëndë në industrinë petrokimike. Në reaksionet katalitike të plasaritjes si kumeni, aktiviteti i katalizatorit të zeolitit Sc-Y është 1000 herë më i lartë se ai i katalizatorit të silikatit të aluminit; Krahasuar me disa katalizatorë tradicionalë, perspektivat e zhvillimit të katalizatorëve të skandiumit do të jenë shumë të ndritshme.
Industria e energjisë bërthamore
Shtimi i një sasie të vogël të Sc2O3 në UO2 në karburantin bërthamor të reaktorit me temperaturë të lartë mund të shmangë transformimin e rrjetës, rritjen e vëllimit dhe çarjet e shkaktuara nga konvertimi i UO2 në U3O8.
Qeliza e karburantit
Në mënyrë të ngjashme, shtimi i 2.5% deri në 25% skandium në bateritë nikeli alkaline do të rrisë jetëgjatësinë e tyre të shërbimit.
Mbarështimi bujqësor
Në bujqësi, farat si misri, panxhari, bizeleja, gruri dhe luledielli mund të trajtohen me sulfat skandiumi (përqendrimi është përgjithësisht 10-3~10-8mol/L, bimë të ndryshme do të kenë ndryshime) dhe është arritur efekti aktual i nxitjes së mbirjes. Pas 8 orësh, pesha e thatë e rrënjëve dhe sythave u rrit me 37% dhe 78% përkatësisht krahasuar me fidanët, por mekanizmi është ende në studim e sipër.
Nga vëmendja e Nielsen ndaj borxhit të të dhënave të masës atomike deri më sot, skandiumi ka hyrë në vizionin e njerëzve vetëm për njëqind ose njëzet vjet, por pothuajse ka qëndruar në bankë për njëqind vjet. Vetëm me zhvillimin e fuqishëm të shkencës së materialeve në fund të shekullit të kaluar, ai i solli vitalitet atij. Sot, elementët e rrallë të tokës, përfshirë skandiumin, janë bërë yje të nxehtë në shkencën e materialeve, duke luajtur role gjithnjë në ndryshim në mijëra sisteme, duke sjellë më shumë komoditet në jetën tonë çdo ditë dhe duke krijuar vlerë ekonomike që është edhe më e vështirë për t'u matur.
Koha e postimit: 29 qershor 2023